Реабилитация при дистальном переломе лучевой кости
Перелом лучевой кости – это самый частый перелом у человека, составляющий 25% от всех переломов костей конечностей. Дистальный метаэпифиз – это нижний конец лучевой кости, расположенный рядом с кистью.
Перелом «луча в типичном месте» обычно возникает при прямом падении на вытянутую руку. Помимо резкой боли в руке, может появиться штыкообразная деформация, изменение положения кисти. В процесс перелома бывают вовлечены нервы и сосуды запястья, которые могут быть зажаты отломками, что проявляется онемением в пальцах, похолоданием кисти.
Для уточнения характера перелома и выбора дальнейшей тактики лечения используется рентгенография, в ряде случаев – компьютерная томография. Иногда требуется УЗИ кистевого (лучезапястного) сустава.
Поскольку лучевая кость примыкает к кисти, очень важно восстановить анатомию и объем движений в суставе, чтобы в дальнейшем избежать проблем с ним. Раньше такие переломы лечили только консервативно, в гипсовой повязке, но часто отломки смещались, кость срасталась неправильно, что в дальнейшем сказывалось на функции конечности – рука не сгибалась и/или не разгибалась до конца – формировалась тугоподвижность сустава (контрактура), оставался болевой синдром. К тому же длительное пребывание в гипсе отрицательно сказывалось на кожных покровах.
Длительность больничного листа при переломе дистального метаэпифиза лучевой кости зависит от рода деятельности пациента. К примеру, для офисных работников средний срок нетрудоспособности – 1,5 месяца. Для профессий, связанных с физической нагрузкой, срок нетрудоспособности может быть больше.
Консервативное лечение перелома лучевой кости (гипсовая или пластиковая повязка)
При переломах без смещения можно применять консервативное лечение – в гипсовой повязке или использовать пластиковый гипс, который более комфортен и не боится воды. Средний срок пребывания в гипсе – около 6 недель. Однако, данный метод лечения имеет свои недостатки – после консервативного лечения сустав требует разработки движений, реабилитации. При лечении перелома даже с небольшим смещением отломков, в гипсе может произойти вторичное смещение отломков из-за особенностей анатомии лучевой кости.
Оперативное лечение перелома лучевой кости (остеосинтез)
Практически все переломы лучевой кости со смещением требуют оперативного лечения – сопоставления и фиксирования отломков кости – остеосинтеза. Именно этот метод позволяет восстановить функцию кисти наиболее полноценно и добиться хороших функциональных результатов.
Лучевая кость первично срастается примерно за 6-8 недель, однако полная перестройка кости продолжается до 2 лет после перелома. Спустя этот срок пациент может начинать полноценно пользоваться рукой. Но разрабатывать руку с помощью определенных, рекомендованных врачом, упражнений, благодаря использованию фиксаторов можно уже в первые сутки после вмешательства. Легкие спортивные физические нагрузки можно начинать примерно спустя 3 месяца после операции.
В зависимости от типа перелома (оскольчатый, многооскольчатый, со значительным или незначительным смещением) можно выделить несколько возможных вариантов фиксации -пластиной, фиксированной винтами; аппаратом внешней фиксации; винтами или спицами.
В ряде случаев при выраженном отеке вначале на кисть накладывается аппарат внешней фиксации, а после спадения отека он заменяется на пластину (или другой фиксатор, в зависимости от типа перелома).
Остеосинтез лучевой кости пластиной
При значительном смещении отломков используется остеосинтез лучевой кости металлической пластиной, специально разработанной для данной области. После сопоставления отломков, пластина фиксируется винтами к поврежденной кости. После установки пластины, на кожу накладываются швы, также применяется гипсовая лонгета. После операции назначается лекарственная терапия: обезболивающие препараты, препараты кальция для стимуляции сращения кости, при необходимости – препараты местного действия для уменьшения отека. Средний срок пребывания в стационаре – 7 дней. Швы снимаются в спустя 2 недели, на контрольном приеме у травматолога, тогда же пациент отказывается и от гипсовой повязки. Рука находится в возвышенном положении на косыночной повязке. Необходимости в удалении пластины, как правило, нет.
Аппарат внешней фиксации
В некоторых случаях – в пожилом возрасте, при выраженном отеке кисти и лучезапястного сустава, делать доступ для установки пластины бывает нежелательно в силу различных факторов (отек, состояние кожи). В таких случаях устанавливают аппарат внешней фиксации – он фиксирует отломки с помощью спиц, которые проходят через кожу в кость. Аппарат выступает над кожей небольшим блоком (около 12 см длиной и 3 см высотой). Преимущество этого вида остеосинтеза в том, что нет необходимости делать большие разрезы кожи, однако за аппаратом нужно следить весь срок его ношения – делать перевязки, чтобы спицы не воспалились.
После операции рука 2 недели находится в гипсовой лонгете, затем пациент начинает разрабатывать лучезапястный сустав в аппарате, который этому не препятствует.
Аппарат внешней фиксации удаляется примерно через 6 недель, после проведения рентген-контроля, в условиях стационара. Перевязки необходимо проводить через день, в амбулаторном режиме. Рука носится в возвышенном положении на косыночной повязке.
Фиксация спицами или винтами
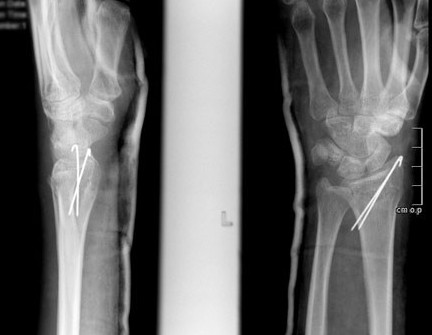
При незначительном смещении отломков лучевая кость фиксируется спицами или винтами через небольшие проколы кожи. По стандартному протоколу, на 2 недели накладывается гипсовая лонгета, затем пациент начинает разрабатывать руку. Спустя 6 недель спицы извлекаются.
В ряде случаев возможно применение саморассасывающихся имплантатов (винтов, спиц), удалять которые не нужно.
Застарелые, неправильно сросшиеся переломы лучевой кости
При застарелых неправильно сросшихся переломах, пациентов могут беспокоить болевые ощущения, присутствовать ограничения движения – тугоподвижность сустава, и другие неприятные последствия (онемение и отечность пальцев кисти). В подобных случаях рекомендовано оперативное лечение, чаще всего – с фиксацией пластиной. Кость разобщается, выставляется в правильное положение и фиксируется. Если есть зона дефекта кости – например, если кость срослась с укорочением, то он заполняется либо собственной костью человека: производится пересадка кости, которая берется, обычно, из гребня подвздошной (тазовой) кости, либо искусственной костью, которая примерно за 2 года перестраивается в собственную костную ткань.
Дальнейшее послеоперационное лечение при застарелых и неправильно сросшихся переломах лучевой кости аналогичны описанным ранее. Однако,может потребоваться более длительная реабилитация.
Анестезия при оперативном лечении перелома дистального метаэпифиза лучевой кости
Для проведения всех вышеописанных операций, как правило, используется проводниковая анестезия – раствор анестетика вводится в зону плечевого сплетения, где проходят нервы, которые отвечают за чувствительность и движения верхней конечности, и рука полностью немеет. Подобная анестезия достаточно легко переносится, длится 4-6 часов. Фактически это разновидность местной анестезии. Кроме того, делается премедикация – успокаивающий укол перед операцией, и во время операции человек спит своим сном. Возможно применение общей анестезии. Окончательный выбор метода анестезии определяется врачом-анестезиологом накануне операции при совместной беседе с пациентом.
Источник
Перелом лучевой кости развивается в том случае, когда человек падает на вытянутую руку. Переломы различаются по направлению и типу перемещения повреждённых фрагментов кости нарушению целостности кожных покровов. Переломы лучевой кости могут быть со смещением и без смещения. В Юсуповской больнице реабилитологи восстанавливают нарушенную функцию верхней конечности после перелома лучевой кости с помощью современных методов реабилитации.
Старший инструктор-методист ЛФК проводит разработку лучезапястного сустава с помощью комплекса гимнастических упражнений. Силу мышц пациенты восстанавливают во время работы на механических и компьютеризированных тренажёрах. Массаж мышц снимает их спазм, способствует восстановлению движений в суставе. Восстановление нарушенной функции конечности проходит быстрее после физиотерапевтических процедур.
Осложнения переломов лучевой кости
Осложнения переломов лучевой кости разделяют на 2 большие группы: непосредственные и отдалённые осложнения травмы. Непосредственные осложнения травмы развиваются из-за влияния повреждений, возникших в результате перелома кости, на нормальное функционирование конечности. Отдалённые последствия травмы представляют осложнения, которые возникли в результате неадекватного лечения или нарушения нормального заживления после травмы.
К непосредственным осложнениям относятся:
- разрывы и травмы нервов, обеспечивающих чувствительность или подвижность конечности;
- травмы сухожилий сгибателей пальцев;
- тугой отёк кисти Турнера;
- повреждение крупных сосудов;
- полный или частный разрыв мышц;
- отрыв мышц от мест крепления к кости;
- острые инфекционные осложнения (при открытых переломах).
К отдалённым последствиям травмы относятся:
- ишемическая контрактура – нарушение подвижности суставов поражённой конечности из-за неверно наложенной гипсовой повязки, которая сдавливает мягкие ткани, нарушая кровоснабжение;
- отдалённые инфекционные осложнения;
- нарушения структуры кости по причине неправильного восстановления костных отломков, не корректно наложенной гипсовой повязки;
- отдалённые последствия гемартроза.
Осложнения перелома лучевой кости усугубляют течение патологического процесса, замедляют образование костной мозоли и восстановление функции верхней конечности. Реабилитологи Юсуповской больницы с первых дней после репозиции костных отломков начинают комплекс лечебной физкультуры и физиотерапевтических процедур, направленных на предотвращение осложнений перелома лучевой кости.
Лечение перелома лучевой кости
Адекватная первая помощь при переломе лучевой кости позволяет избежать осложнений травмы и ускорить восстановление после перелома лучевой кости со смещением. Задачей первой помощи является уменьшение боли, обеспечение покоя пораженной конечности, предотвращение повреждения мягких тканей, которые окружают место перелома. При закрытом переломе конечность фиксируют с помощью лонгеты. Если перелом открытый, останавливают кровотечение и накладывают асептическую повязку на рану, затем выполняют иммобилизации. При переломе лучевой кости со смещением не надо пытаться на месте происшествия восстановить нормальное положение костных отломков, чтобы не повредить окружающие ткани, сосуды и нервы.
В травмпункте пациентам с переломом лучевой кости оказывают первую врачебную помощь. Травматолог проводит оценку состояния пострадавшего с целью определения объёма дальнейшего лечения и предотвращение развития осложнений. После подтверждения факта перелома восстанавливают анатомическую и функциональную целостность травмированной конечности и иммобилизируют руку для того чтобы предотвратить смещения фрагментов сломанной кости.
Травматолог сопоставляет костные фрагменты, фиксирует гипсовой или полимерной повязкой. Врачи при некоторых видах переломов лучевой кости выполняют закрытую или открытую репозицию с последующей фиксацией спицами, накладывают аппарат внешней фиксации. После лечения пациенты нуждаются в восстановлении нарушенной функции верхней конечности.
Реабилитация после перелома лучевой кости
Полное выздоровление после перелома лучевой кости заключается в восстановлении структуры кости, функции конечности (подвижности и чувствительности). Даже при абсолютно адекватном лечении длительное сохранение неподвижности в суставах и мышцах верхней конечности приводит к тому, что пациенту трудно совершать движения, в суставах, которые раньше были ему доступны. Процесс восстановления после травмы занимает длительное время, требует от пациента терпения и желания работать.
Реабилитологи Юсуповской больницы начинают разрабатывать суставы и мышцы при переломе лучевой кости как можно раньше. Сроки начала реабилитационных мероприятий зависят от вида перелома, метода лечения. Если перелом лечат консервативно, то через 3-5 дней, после того, как спадёт отёк, начинают заниматься пальцами кисти.
Вначале выполняют пассивные движения. Берут здоровой рукой палец на сломанной конечности и аккуратно начинают его сгибать во всех суставах. Таким способом разминают по 5-7 минут 3 раза в день все пальцы, кроме большого. Через неделю такой тренировки переходят к активным движениям. Пациент может начинать самостоятельно, без помощи второй руки сгибать пальцы. Очень важно правильно распределять нагрузку. Если в ходе упражнения появилась боль или снова появился отёк, упражнения следует прекратить.
Одновременно с началом пассивных движений в пальцах кисти, приступают к активным движениям в локтевом и плечевом суставах. Пациент поднимает и опускает руку, сгибает её в локте. Делают эти упражнения по 3-5 минут не реже чем 2 раза в сутки, постепенно наращивая нагрузку. Через 3-4 недели, если активные движения пальцами кисти не вызывают боли, начинают увеличивать нагрузку на эти суставы. Нужно взять комок пластилина и разминать его в кулаке. Это упражнение надо делать по возможности часто, в течение недели. После снятия гипса переходить к упражнениям с кистевым эспандером. Заниматься следует не меньше трёх раз в день по 5-7 минут.
Инструктор ЛФК обучает пациента упражнениям на мелкую моторику. К концу четвёртой недели пациент может начинать рисовать или писать поражённой рукой. Можно перебирать по одному зёрнышку рисовую или гречневую крупу. Это позволит сохранить не только силу и подвижность суставов, но и координацию движений пальцев кисти. Можно в качестве упражнения на координацию печатать тексты на клавиатуре компьютера. Если пациент делает упражнения в то время, когда у него установлена гипсовая лангета, то после её снятия, срок реабилитации значительно сократится.
Упражнения должны захватывать все суставные соединения травмированной конечности. Важно регулярно проводить разминку пальцев. Для снятия напряжения в пострадавшей конечности некоторые занятия после снятия гипсовой повязки следует проводить в воде. Продолжительность курса лечебной физкультуры реабилитологи Юсуповской больницы определяют индивидуально. Средняя продолжительность курса лечебной гимнастики составляет 1, 5 месяца.
Реабилитологи обучают пациентов упражнениям, которые можно выполнять дома. Водная гимнастика подразумевает проведение простых упражнений лечебной физкультуры в воде. Занятия можно проводить в ванной. В тёплую воду следует добавить косметическую морскую или пищевую соль. Она упростит процесс проделывания упражнений.
Комплекс состоит из следующих упражнений:
- сгибательные и разгибательные движения ладонями в воде;
- круговые движения кисти;
- повороты в локтевом суставе;
- сжатие и разжимание ладони в кулак.
Продолжительность процедуры от 10 до15 минут. Рекомендуется ежедневно делать 2-3 подхода.
Рекомендованный инструктором комплекс ЛФК пациенты также могут выполнять дома. Следует принять исходное положение «сидя за столом». На столе нужно расположить локти, а под кисти рук подложить тонкую, плоскую подстилку. Кисти необходимо сгибать и разгибать, проделывать вращательные движения. Расположите кисти на столе ребром, а затем наклоняйте руку так, чтобы поверхности стола в начале коснулся мизинец, а затем последовательно все пальцы. Уприте локти о стол, сомкните ладони и наклоняйте их поочерёдно к левому и правому запястью.
ЛФК при переломе лучевой кости
В процессе восстановления функции верхней конечности после перелома лучевой кости важную роль играют тепловые процедуры. Физиотерапевты Юсуповской больницы проводят прогревание самыми разными способами (парафиновыми или озокеритовыми аппликациями). К комплексу гимнастических упражнений добавляют массаж. Для лечения перелома лучевой кости используют следующие процедуры:
- электромагнитное поле ультравысокой частоты (в ходе процедуры ткани поражённой конечности начинают нагреваться, пациент чувствует тепло, ускоряется регенерация, боль слабеет);
- электромагнитного поля низкой частоты – уменьшает отёк, ослабевает дискомфорт и боль;
- ультрафиолетовое облучение способствует увеличению синтеза витамина D, который необходим для всасывания кальция из пищи в пищеварительном тракте;
- электрофорез кальция на область травмы способствует ускорению образования костной мозоли и облегчает восстановление повреждённой костной ткани.
Пройти курс восстановления после перелома лучевой кости по доступной цене можно в клинике реабилитации. Контакт центр работает круглосуточно 7 дней в неделю. Звоните по телефону Юсуповской больницы и запишитесь на примем.
Источник
Каракулько Н.А., Рузанов В.И.
Введение. Переломы дистального метаэпифиза лучевой кости являются наиболее частыми повреждениями верхней конечности у взрослых (15 – 33%) [2,4]. Наиболее тяжелые внутрисуставные нестабильные повреждения диагностируются в 50-55% случаев [1,3]. Данные переломы нередко сопровождаются различными осложнениями, специфика которых предопределяется морфологией повреждения, используемыми методами лечения и нарушениями лечебно-реабилитационного режима [5,17]. Сохраняется высокий риск возникновения вторичного смещения отломков (16,5 – 58,3%) [6]. В результате нестабильных переломов неправильное сращение достигает 89% и сопровождается угловой и ротационной деформацией, укорочением лучевой кости и импакцией локтевой кости в запястье, что приводит к развитию и прогрессированию стойких нарушений функции лучезапястного сустава, дегенеративных процессов [13]. Актуальность проблемы возрастает в связи с длительными сроками реабилитации при общепринятых методах восстановительного лечения, достигающих более одного года [8]. В связи с этим ведутся исследования по совершенствованию тактики лечения путем разработки дифференцированных подходов к выбору метода лечения, с учетом особенностей отдельных видов переломов, приобретенного опыта и общего состояния пациента [7,12]. Хирургическое лечение обрело популярность в настоящее время в основном благодаря двум аспектам: восстановлению анатомии, а также раннему функциональному послеоперационному лечению [20]. В зависимости от тяжести модели перелома и ассоциирующихся повреждений, диапазон выбора метода лечения велик – от сугубо консервативной позиции A. Colles (1814) до современного, фактически безальтернативного предпочтения хирургической тактике [21]. Опорные пластины, стягивающие винты, спицы Киршнера, аппараты наружной фиксации различной модификации, цементная фиксация – всё находит свое применение в лечении различных конфигураций данных переломов.
В большинстве случаев лечения внутрисуставных повреждений дистального отдела костей предплечья требуется использование губчатой аутопластики для восстановления суставных поверхностей, поскольку при «поднятии» и репозиции вдавленных фрагментов образуется метаэпифизарный дефект [18]. Всё большее предпочтение травматологи отдают накостному остеосинтезу пластинами с угловой стабильностью в комбинации с костной пластикой. Данный метод осуществляет прямую визуализацию и редукцию, стабильную внутреннюю фиксацию и раннюю мобилизацию во время периода биологического заживления кости [14]. Однако вопрос возмещения костного дефекта метаэпифизарной зоны до настоящего времени не решен. Использование кортико-спонгиозного аутотрансплантата из гребня подвздошной кости, хотя и признано «золотым стандартом», однако имеет такие недостатки как боль в донорской зоне, риск повреждения кожного нерва в области забора трансплантата, увеличение продолжительности операции, риск развития инфекционных осложнений в ране и необходимость углубления наркоза, что особенно нежелательно при лечении пациентов пожилого возраста [9,20,21]. В качестве альтернативных источников для заполнения дефекта лучевой кости применяют: биологическую кость «Bio-Oss Geistlich», синтетическую кость «chronOS», гидроксиапатита карбонат, костный цемент, содержащий фосфат кальция, костный цемент «Norian SRS» и другие виды материалов [9]. Однако перестройка этих трансплантатов все же происходит медленнее, чем перестройка аутокости, что затрудняет своевременное восстановление функции поврежденной конечности. Применение аппарата наружной фиксации для формирования костного регенерата не всегда позволяет в полной мере восстановить анатомию лучевой кости [19]. Нами был разработан новый способ комбинированного лечения внутрисуставных повреждений дистального отдела лучевой кости с использованием аутопластики дефекта метаэпифизарной зоны губчатым трансплантатом, перемещенным из шиловидного отростка лучевой кости (патент РФ на изобретение № 2453288 от 09.03.2011) [11].
Цель исследования: оценка нового способа хирургического лечения больных с внутрисуставными переломами дистального отдела лучевой кости с дефектом метаэпифизарной зоны.
Материалы и методы. За период с 2009 по 2011 г. ФГБУ «СарНИИТО» Минздрава России были прооперированы 20 пациентов с внутрисуставными переломами дистального метаэпифиза лучевой кости (12 женщин и 8 – мужчин) в возрасте от 20 до 70 лет (в среднем 34,6) с использованием разработанного нами способа. В 11 случаях пациенты получили травму в результате падения при ходьбе, в 9 случаях имела место высокоэнергетическая травма (дорожно-транспортная, падение с высоты). Всем пациентам было проведено двухэтапное оперативное лечение с использованием костной пластики дефекта и накостного шинирования. По классификации Fernandez переломы относились к типу 3 (компрессионные внутрисуставные) – у 6 (30%) пациентов, к типу 4 (переломовывихи) – у 2 (10%), к типу 5 (внутрисуставные с отрывом костных фрагментов) – у 7 (35%), к типу 6 (неправильно сросшиеся переломы и ложные суставы) – у 5 (25%), репозиция которых сопровождалась образованием костного дефекта в метаэпифизарной зоне, требующего его замещения. Сроки от момента травмы до операции составили в среднем 3,5 недели (от 0,5 до 12,6 недель). У всех больных были нарушения конгруэнтности суставных поверхностей лучезапястного сустава, укорочение лучевой кости, резкое ограничение функции лучезапястного сустава. Средние значения рентгенометрических и функциональных показателей кистевых суставов до оперативного лечения составляли: ЛЛУ (лучелоктевой угол) – 15,6±4,4˚; ЛИ (ладонная инклинация) – 15,5±6,9˚; ЛЛИ (лучелоктевой индекс) – 4,8±2,3˚. В среднем ООД (общий объем движений) в кистевых суставах составлял 52,6±10,5% от показателей здоровой конечности. Остеосинтез выполняли с помощью пластин с угловой стабильностью DVR производства DeРuy и пластин с угловой стабильностью производства ChM. Лечение внутрисуставных переломов заключалось в комбинированном хирургическом пособии с использованием ауто-аллопластики костного дефекта. Показаниями к операции являлись признаки нестабильности перелома, выраженная деформация лучезапястного сустава и нарушение функции предплечья и кисти.
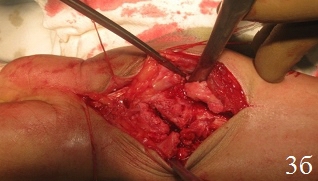
Техника операции. После предоперационной подготовки больного укладывали на ортопедическом столе на спине, поврежденную конечность – на дополнительном столике в положении руки на тыльной поверхности, в область лучезапястного сустава подкладывали валик. Первым этапом производили восстановление длины лучевой кости путем наложения на предплечье и кисть монолатерального стержневого аппарата внешней фиксации и проведения одномоментной дистракции периферических отломков под рентгенологическим контролем, используя принцип лигаментотаксиса (рис. 1а). Функцией аппарата наружной фиксации, прежде всего, являлись нейтрализация сил компрессии и сведение к минимуму мышечно-сухожильной тяги, которая приводит к укорочению лучевой кости. Однако осевая тракция не оказывает влияние на волярный угол. Известно, что ладонная лучезапястная связка короче и толще, чем тыльная, которая по площади более протяженная, имеет z-образную форму и редко натягивается, поэтому в условиях тракции по оси, возникает тенденция к увеличению тыльного запрокидывания. В связи с этим наложение дистракционного аппарата являлось 1-м этапом операции для восстановления нормальной длины лучевой кости. Затем проводили хирургический ладонный доступ с возможностью обеспечения переднего обнажения дистального отдела лучевой кости. Осуществляли репозицию внутрисуставных отломков путем их выпрессовывания из метаэпифизарной зоны лучевой кости и прижатия к суставной поверхности проксимального ряда костей запястья (рис. 1б). Образовавшийся во время репозиции костный дефект заполняли аутотрансплантатом. Забор трансплантата производили из проведенного ранее разреза. Для этого производили остеотомию кортикальной пластины шиловидного отростка лучевой кости с её волярной поверхности размерами порядка 1 см2. Кортикальную пластину откидывали кнаружи. С помощью ложки Фолькмана осуществляли забор трансплантата в виде губчатого вещества лучевой кости и производили перемещение его в зону костного дефекта. С помощью элеватора проводили запрессовку трансплантата в зону костного дефекта с обеспечением возможности восстановления и укрепления суставной поверхности лучевой кости и ее медиальной колонны, создавая дополнительную фиксацию – подпору для мелких отломков.
Образовавшийся дефект шиловидного отростка лучевой кости после забора трансплантата заполняли биодеградирующим костно-замещающим препаратом с высокими упруго-прочностными свойствами и закрывали остеотомированной кортикальной пластиной волярной поверхности шиловидного отростка с возможностью создания дополнительной опоры латеральной колонне, являющейся основной костной опорой кисти и местом прикрепления большинства связок. После этого производили фиксацию отломков с помощью пластины с угловой стабильностью (рис.1г). Завершали установку пластины путем введения двух винтов через отверстия пластины, костно-замещающий препарат и трансплантат. Первый винт вводили в проксимальное отверстие пластины с возможностью формирования щели между средней частью пластины и лучевой костью, что обеспечивало эффект разгрузки проксимального фрагмента лучевой кости после введения винтов. Второй винт вводили таким образом, чтобы пластина была плотно прижата к диафизу лучевой кости, что обеспечивало эффект разгрузки дистального фрагмента лучевой кости. Подшивали квадратный пронатор с обеспечением укрытия пластины и защиты мягкотканых структур. Рану послойно ушивали наглухо. В заключение операции осуществляли демонтаж аппарата внешней фиксации. Особенностями ведения послеоперационного периода являлась ранняя функциональная нагрузка на суставы конечности. Внешнюю иммобилизацию (тыльная гипсовая лонгета) оперированной конечности проводили в течение 1 суток после операции с целью купирования болевого синдрома. В дальнейшем дополнительной иммобилизации не требовалось. Разработку движений в межфаланговых суставах пальцев и лучезапястном суставе начинали в 1-2 сутки после операции. Послеоперационный период у всех больных протекал без осложнений.
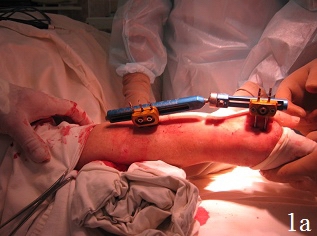
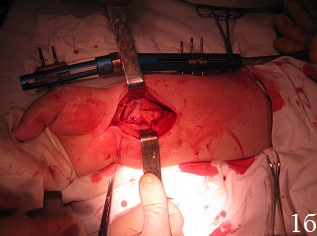
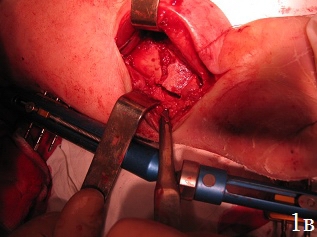
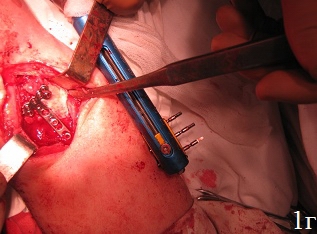
Рис. 1. Этапы операции: а – восстановление длины лучевой кости путем наложения дистракционного аппарата внешней фиксации, б – открытая репозиция, забор трансплантата, в – запрессовка трансплантата в зону дефекта, г – пластика костного дефекта донорской зоны костно-замещающим материалом, остеосинтез пластиной с угловой стабильностью
Результаты и обсуждение. Результаты лечения оценивали через 3, 6, 12 месяцев по объективным и субъективным критериям (методика, разработанная О.М. Семенкиным и С.Н. Измалковым [10]; функциональная способность кисти – опросник НФПКЛ (неспособность функции предплечья, кисти, лучезапястного сустава), основой для которого послужил адаптированный опросник DASH; оценка качества жизни – опросник SF-36 (health us survey). Максимальные сроки наблюдения составили 2 года.
Сращение костных отломков лучевой кости происходило в среднем через 2,6±0,3 месяца после операции. Через год средние величины рентгенометрических показателей приближались к нормальным и составляли: ЛЛУ (лучелоктевой угол) =25,6±4,8˚; ЛИ (ладонная инклинация) =8,5±6,9˚; ЛЛИ (лучелоктевой индекс) =0,8±1,3˚. В среднем ООД (общий объем движений) в кистевых суставах составлял 87,6±3,5%. Ни в одном из представленных клинических случаев не было зафиксировано перелома лучевой кости в области забора трансплантата, его миграции и вторичного смешения отломков. Из 20 больных у 19 получен хороший результат, у 1 – удовлетворительный. В одном случае развилась невропатия срединного нерва, которая потребовала его невролиза.
Клинический случай 1. Б-й С., 37 лет. Диагноз: Неправильно сросшийся внутрисуставной перелом дистального метаэпифиза левой лучевой кости, лучевая косорукость. Ложный сустав шиловидного отростка левой лучевой кости, вывих головки левой локтевой кости (рис. 2 а). Поступил спустя 3 месяца поле травмы с жалобами на деформацию левого предплечья с выраженным нарушением функции. Больному выполнен остеосинтез по разработанному способу (рис. 2 б,в). Послеоперационный период протекал без осложнений. Со 2-го дня после хирургического вмешательства больному проводили лечебную гимнастику для суставов кисти и пальцев. На 10-й день после хирургического вмешательства больной был выписан. К работе приступил через 6 недель после хирургического вмешательства. На контрольном осмотре через год после хирургического вмешательства: рентгенометрические показатели: общий объем движений в кистевом суставе составил 89,6% от здоровой кисти, безболезненный. На рентгенограммах дистального отдела предплечья было отмечено: полное восстановление конгруэнтности суставных поверхностей лучезапястного сустава, полная консолидация отломков лучевой кости, без потери репозиции.
Клинический случай 2. Б-й Ф., 46 лет, Диагноз: Ложный сустав дистального метаэпифиза левой лучевой кости, вывих головки локтевой кости, лучевая косорукость (рис. 3 а,б). Больному выполнен остеосинтез по разработанному способу (рис. 3 в,г). Пациенту проводилось местное лечение: перевязки послеоперационной раны растворами антисептика; с целью профилактики инфекционных осложнений в течение 5 дней проводилась антибактериальная терапия. Гипсовая иммобилизация в первые сутки после операции. Разработку движений в межфаланговых суставах пальцев и лучезапястном суставе начинали на 1-2 сутки после операции. К работе приступил через 8 недель после хирургического вмешательства. На контрольном осмотре через год после хирургического вмешательства: рентгенометрические показатели: общий объем движений в кистевом суставе составил 87,6% от здоровой кисти, безболезненный. На рентгенограммах дистального отдела предплечья было отмечено: восстановление конгруэнтности суставных поверхностей лучезапястного сустава, полная консолидация отломков лучевой кости, без потери репозиции.
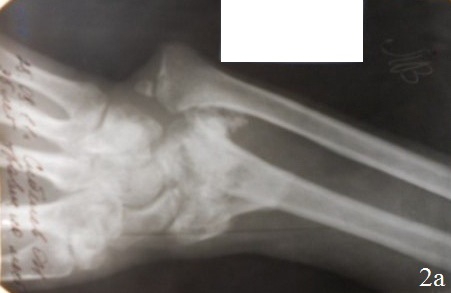
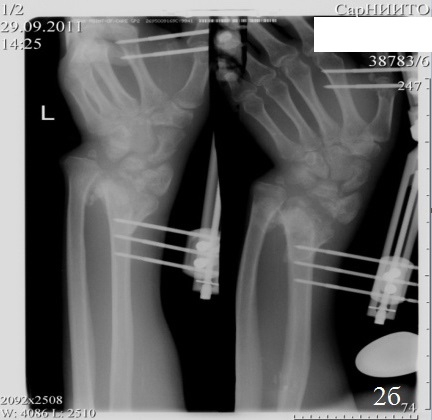
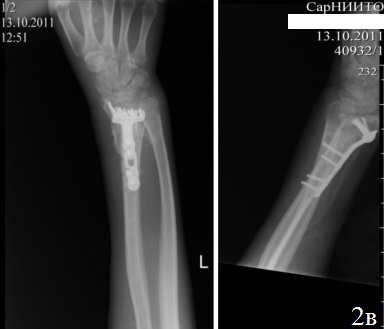
Рис. 2. Рентгенограммы кистевого сустава больного С., 37 лет: а – до операции, б – во время первого этапа операции, в – после остеосинтеза
По данным J. Patel [16], из 1670 случаев взятия аутотрансплантата из дистального метаэпифиза лучевой кости осложнения составили 4%, в том числе, переломы лучевой кости – 2,3%. Экспериментальные исследования L. Horne [15] показали, что после забора менее 25% объема спонгиозного вещества из дистального метафиза лучевой кости не выявлено значимого различия в прочности лучевой кости при ее осевой компрессии по сравнению с неизмененной контралатеральной конечностью (p = 0,273). В наших наблюдениях донорская зона забора трансплантата была возмещена костно-замещающим препаратом с высокими упруго-прочностными свойствами, что обеспечивало создание дополнительной опоры латеральной колонне, являющейся основной костной опорой кисти. Не было зафиксировано ни одного случая перелома лучевой кости в донорской зоне, вторичного смещения отломков и нарушения стабильности системы «фиксатор-кость».
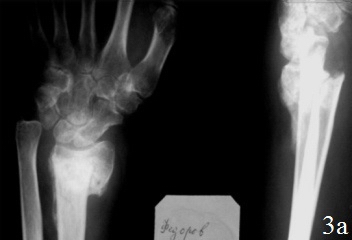

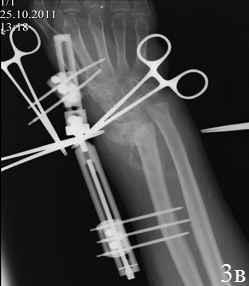
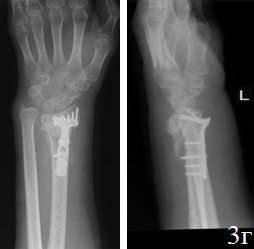
Рис. 3. Рентгенограммы кистевого сустава б-го Ф.: а – после 3,5 месяцев консервативного лечения,


