Ушибы головного мозга корниенко
Мы уже писали о лучевой диагностике черепно-мозговой травмы. В этой статье подробно рассматривается визуализация одного из вида черепно-мозговых травм – ушиба головного мозга.
Ушиб головного мозга на КТ
Что такое ушиб головного мозга? Ушиб, или контузия мозга – это механическое повреждение вещества мозга в виде его размозжения, нарушение строения, образование зоны детрита, а также кровоизлияние в зону детрита. Ушиб мозга – это опасное состояние, требующее срочной госпитализации в нейрохирургический (в крайнем случае, в неврологический стационар).
Ушиб мозга может сопровождаться опасными осложениями, угрожающими жизни больного – вклинением и смещением (дислокацией) мозга. Основные типы вклинений: вклинение поясной извилины под серп большого мозга, височно-тенториальное вклинение, мозжечково-тенториальное вклинение, вклинение миндалин мозжечка в большое затылочное отверстие.
При подозрении на ушиб мозга необходимо делать компьютерную томографию (КТ) головного мозга. Она позволяет точно установить наличие ушиба, оценить его размеры, исключить вклинение и смещение головного мозга. МРТ головного мозга более информативна при оценке отдаленных последствий ушиба, развития остаточных кистозно-глиозных и атрофических изменений.
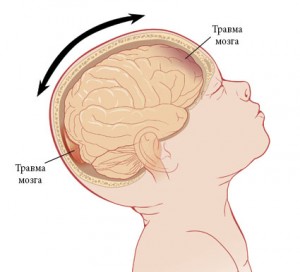
Ушиб мозга возникает как в зоне удара, так и с противоположной стороны черепа – в зоне противоудара.
КТ-признаки ушиба мозга
Что видно на КТ при ушибе мозга? На компьютерных томограммах очаг ушиба (контузии) выглядит как чередующиеся гиперденсивные участки (гематомы) и гиподенсивные (детрит). Контузионные очаги формируются как на стороне удара (приложения силы), так и на стороне противоудара. Перифокальная ишемия от сдавления сосудов гематомой увеличивает зону патологически измененных тканей, обуславливает выраженность дислокаций мозга.
Существующая классификация ушибов мозга по Корниенко, принятая не повсеместно, предусматривает четыре типа очагов: контузии первого типа выглядят как однородные гиподенсивные участки и внешне очень схожи с инфарктом мозга. Ушибы второго типа выглядят «пестрыми» из-за множественных гематом небольшого размера, располагающихся в зоне детрита. Контузии третьего типа – крупные множественные гематомы на фоне детрита, и ушибы четвертого типа представляют собой собственно паренхиматозную гематому.
Наиболее часто встречающиеся очаги контузии по типу внутримозговой гематомы эволюционируют следующим образом: в период 1-3 суток вокруг гематомы возникает гиподенсивная зона, обусловленная перифокальным отеком мозга, затем в период от нескольких недель до месяца происходит лизис гематомы и рассасывание крови, обратное развитии ишемических изменений. Итогом может стать формирование кисты либо глиального рубца.

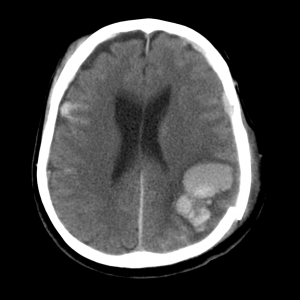
Признаки ушиба мозга на КТ. Очаг контузии мозга по типу паренхиматозной гематомы, окруженной зоной перифокального отека. С противоположной стороны также можно заметить очаг контузии и участок субарахноидального кровоизлияния.
Диффузное аксональное повреждение (ДАП)
В развитии диффузного аксонального повреждения основную роль играет различная плотность (и вес) белого вещества и коры головного мозга. Тело клетки (дендрит) располагается в сером веществе, аксон в белом. При резком ускорении либо замедлении серое и белое вещество движутся с разной скоростью, в результате чего происходит сдвиг серого вещества относительно белого, следствием чего является фрагментирование нейронов: тело отрывается от аксона. Происходит также разрыв капилляров на границе коры и белого вещества.
На КТ изменения при диффузном аксональном поражении в большинстве случаев неразличимы, можно обнаружить лишь гематомы различного размера в веществе мозга, а также признаки его отека. Неопытный рентгенолог может пропустить ДАП на компьютерных томограммах.
По локализации (и степени тяжести) ДАП может быть трех различных типов: с локализацией в лобных долях, паравентрикулярно, в области наружной и внутренней капсулы, в мозжечке (1-й тип); с локализацией как и в предыдущем случае, а также в мозолистом теле (2-й тип); так же, как и в предыдущем случае, но с распространением на дорсолатеральные участки мозгового ствола, ножки мозжечка, с нарушением кортикально-спинальных трактов (3-й тип).
Крайне важно, чтобы снимки КТ головного мозга при его ушибе оценивал настоящий специалист. Если этого не происходит, результаты КТ могут быть сомнительны. В таких случаях может помочь экспертный пересмотр результатов КТ. Сегодня снимки в электронном виде можно отправить врачу в любую точку земного шара, и Второе мнение (second оpinion) – активно развивающееся направление диагностики. В России существует организация Национальная телерадиологическая сеть – система консультаций по КТ, МРТ, ПЭТ-КТ и другим диагностическим изображениям. С помощью этой системы можно отправить результаты КТ головного мозга на пересмотр в Институт мозга человека, и получить через 24 часа подробное независимое заключение.
Кандидат медицинских наук, член Европейского общества радиологов
Источник
Компьютерная томография (КТ) в настоящее время является ведущим в диагностике черепно-мозговой травмы. Возможность прижизненной визуализации мягких тканей, костей, мозговой паренхимы, ликворных пространств, инородных тел и других составляющих черепно-мозговой травмы при КТ открыла новые пути развития нейротравматологии. Широкое распространение получила КТ и в детской нейротравматологии
Ушибы мягких тканейхарактеризуются увеличением объема, сочетанием с участками повышенной плотности в результате пропитывания их кровью. Подапоневротические гематомыотличаются зонами повышенной плотности в ранние сроки после травмы, которые располагаются над костными структурами.
Переломы костей черепавизуализируются при КТ в костном режиме. Линейные переломы представлены в виде полосок просветления, а вдавленные переломы в виде смещения фрагментов кости в полость черепа (Рис.7.22).
Ушибы головного мозгав зависимости от тяжести (выраженности) деструктивных изменений мозговой ткани обычно разделяют на 3 типа. Частота их выявления увеличивается с увеличением срока после травмы. По данным Егуняна М.А., в первые сутки после травмы КТ признаки ушиба мозга обнаруживаются у 23% обследованных детей, кроме того у 18% обнаруживаются признаки отека мозга с сужением субарахноидальных пространств и желудочков мозга. На 2 – 3 сутки ушибы мозга выявляются уже у 33,3% пострадавших, при наличии признаков отека мозга еще у 11,1%. На 4 – 7 сутки эти цифры поднимаются до 66,6% и 33,4%.
Ушибы мозга легкой степени тяжести (ушибы I типа)представлены небольшими зонами пониженной плотности мозгового вещества (18 – 25 ед.Н) или участками изоденсивными мозгу с наличием небольшого объемного эффекта позволяющие говорить об ушибе мозга. Эти ушибы достаточно быстро (2-6 дней) подвергаются обратному развитию и обычно занимают кортикальную зону конвекситальных отделов полушарий мозга, часто сочетаясь с переломами костей и подапоневротическими гематомами.
Ушибы мозга средней степени тяжести (ушибы IIтипа)характеризуются наличием контузионных очагов повышенной плотности (до 60 ед.Н) или зонами пониженной плотности с некомпактными вкраплениями участков повышенной плотности (Рис.7.2, 7.24). Степень сопутствующего отека мозга и объемного эффекта большая. Эти очаги ушиба также достаточно быстро (в течение 10 – 14 дней) подвергаются обратному развитию, что говорит об отсутствии значительной деструкции мозгового вещества, но атрофические изменения в мозге обнаруживаются почти постоянно.
Ушибы мозга тяжелой степени тяжести (ушибы III типа)представлены зонами неравномерно повышенной плотности (65 – 75 ед. Н), которые чередуются с участками пониженной плотности (Рис. 7.25).
Данный вид ушиба мозга соответствует патологоанатомическому определению «очаг размозжения мозга». Они сопровождаются выраженным перифокальным отеком, нередко имеющего тенденцию к генерализации на 3 – 4 сутки. Исчезновение геморрагического компонента очагов ушиба 3 вида происходит на 2 – 3 недели, хотя явления отека сохраняются на более длительный срок.
Корниенко В.Н. с соавт. предложили разделять 4 вида очагов ушиба мозга, при этом выделив ушибы IV вида – внутримозговые гематомы или очами ушибов с превалированием геморрагического компонента над мозговым детритом (Рис. 7.26).
Очень интересны сопоставления типов ушибов мозга и летальности, проведенные LankschW. С соавт. Установлено, что летальность при ушибах I типа не превышает 7% наблюдений, при ушибах II типа она составляет 41% и при ушибах III типа достигают 70% наблюдений.
Диффузные аксональные повреждения мозгана КТ характеризуются общим увеличением объема мозга, как результат диффузного отека или набухания мозга с мелкоточечными очагами геморрагии в мозолистом теле, стволовых или перивентрикулярных структурах.
Субарахноидальные кровоизлияниянаиболее частый вид травматических внутричерепных кровоизлияний, особенно при тяжелой черепно-мозговой травме. КТ признаком субарахноидального кровоизлияния является повышение плотности конвекситальных субарахноидальных пространств, боковых щелей мозга, базальных цистерн (Рис.7.27). Учитывая быстроту резорбции крови из ликворных пространств, КТ диагностика субарахноидальных кровоизлияний наивысшая в первые часы после травмы. В течение первых двух суток частота обнаружения КТ признаков геморрагии снижается на половину.
Эпидуральные гематомыпредставлены обычно зонами повышенной плотности двояковыпуклой формы, прилежащей к костям свода черепа (Рис. 7.28). Зоны распространения эпидуральных гематом обычно ограничены черепными швами.
Степень повышения плотности изображения гематомы соответствует количеству свернувшейся крови, но при наличии несвернувшейся крови и при резорбции гематомы более 14 дней возможно ее изоденсивное с мозгом изображение. В этих случаях только косвенные признаки (смещение твердой мозговой оболочки, смещение мозга) или внутривенное введение контрастного вещества позволяют правильно установить диагноз.
Субдуральные гематомыхарактеризуются серповидной зоной повышенной плотности, захватывающей значительные участки над полушариями мозга (Рис.7.29), сочетаясь с его сдавлением и смещением срединных структур. В результате резорбции крови субдуральные гематомы в течении нескольких недель становятся изоденсивными, что затрудняет их диагностику особенно при двухсторонней локализации. Эта локализация очень часто наблюдается у детей грудного возраста. Именно у них нередко возникает необходимость в дифференциальной диагностике между хроническими субдуральными гематомами и хроническими гидромами в результате атрофических изменений в мозге (Рис.7.30, 7.31). Односторонние хронические субдуральные гематомы в зависимости от сроков существования и степени резорбции крови представлены гипер- , гипо- или изоденсивными экстрацеребральными зонами с выраженным смещением мозга (Рис. 7.32).
Особую группу составляют больные с хроническими оссифицирующимися субдуральными гематомами при огромных размерах которых степень смещения мозговых структур и желудочков мозга может быть самой различной от незначительной (Рис.7.33) до резко выраженной (Рис. 7.34).
Внутримозговые гематомычаще встречаются у детей школьного возраста и на КТ представляют собой очаги гомогенно повышенной плотности округлой, овальной или неправильной формы (65 – 75 ед. Н). Очень быстро вокруг гематомы формируется зона отека, достигающая максимума на 2 – 3 сутки и имеющего тенденцию к генерализации (Рис. 7.35). Резорбция крови и снижение плотности очага кровоизлияния обычно происходит к концу месяца.
Внутрижелудочковые гематомыу детей как изолированная форма внутричерепной посттравматической геморрагии встречается крайне редко. Они наблюдаются при очень тяжелой травме как один из компонентов множественных гематом. Внутрижелудочковые кровоизлияния только в том случае может считаться гематомой, если кровь по объему превысила размеры желудочка и произошла тампонада его кровью. На КТ внутрижелудочковые гематомы представлены высокоинтенсивным сигналом, формирующим слепок расширенного желудочка мозга. Чаще обнаруживаются внутримозговые гематомы с прорывом крови в желудочки мозга разной степени выраженности (Рис. 7.36).
Как уже указывалось, практически только у детей встречаются поднадкостнично-эпидуральные гематомы. Их компьютерная диагностика не представляет больших сложностей, а обнаруживаемые изменения весьма характерны для экстра-интракраниальных объемных поражений, разделенных костной структурой. Гематомы могут располагаться одна над другой, принимая вид шара, мяча, или в виде гантелей со смешением основных масс гематом в сторону (Рис.7.37). При специальных исследованиях удается обнаружить и зону линейного перелома кости.
Значительно расширились возможности КТ с внедрением в практику спиральных рентгеновских компьютеров. Если раньше для получения объемного изображения (трехмерная КТ реконструкция) требовалось много времени и больной получал большую лучевую нагрузку, современные аппараты позволяют провести исследование за несколько минут. Особенно важна трехмерная КТ реконструкция при сложных переломах и дефектах черепа, во многом определяя хирургическую тактику (Рис.7.38).
Рис.7.22. КТ (костный режим) ребенка П., 7 лет. Вдавленный многооскольчатый перелом правой лобной кости.
Рис. 7.23. КТ ребенка З., 3 года.
Ушиб лобной области средней степени тяжести без выраженной дислокации и отека мозга.
Рис.7.24. КТ ребенка Н., 12 лет.
Ушиб лобных долей средней степени тяжести (через неделю после травмы). Выраженный отек лобных долей, начинающаяся атрофия левой лобной доли.
Рис.7.25. КТ ребенка А., 7 лет.
Ушиб левой лобной доли тяжелой степени тяжести. Умеренно выражен дислокационный синдром и отек мозга.
Рис. 7.26. КТ ребенка Р., 5 лет.
Ушиб тяжелой степени тяжести лобных долей, больше справа, с преобладанием геморрагического компонента.
Рис.7.27. КТ ребенка Б., 2 года.
Ушиб мозга средней степени тяжести, субарахноидальная геморрагия с распространением крови в межполушарную щель и субарахноидальные пространства правой лобно-теменной области.
Рис.7.28 КТ ребенка Ф., 6 лет.
Эпидуральная гематома левой височной области без значительного дислокационного синдрома.
Рис.7.29. КТ ребенка Т., 3 года.
Острая субдуральная гематома над правым полушарием, выраженное сдавление мозга.
Рис.7.30. КТ ребенка С., 4 года. Двусторонние хронические субдуральные гематомы.
Рис.7.31. КТ ребенка С., 1 год.
Массивные хронические субдуральные гидромы, гипоксическая атрофия мозга.
Рис.7.32. КТ ребенка Б., 9 месяцев.
Хроническая субдуральная гематома левой лобно-теменно-височной области, выраженный дислокационный синдром.
Рис.7.33. КТ ребенка Е., 8 лет.
Оссифицированная хроническая субдуральная гематома правой лобно-теменной области, состояние через 3 года после ликворошунтирующей операции и год после легкой черепно-мозговой травмы. Дислокационный синдром слабо выражен.
Рис.7.34. КТ ребенка М.., 5 лет.
Оссифицирующаяся хроническая субдуральная гематома левой лобно-теменно-височной области, состояние через год после ликворошунтирующей операции. Дислокационный синдром резко выражен.
Рис. 7.35. КТ ребенка Р., 4 года.
Внутримозговая гематома правой височно-подкорковой области со слабо выраженным
дислокационным синдромом.
Рис. 7.36. КТ ребенка Т., 9 лет.
Внутримозговая гематома правой височной области с прорывом крови в тело и задний рог правого бокового желудочка. Умеренно выражен перифокальный отек.
Рис. 7.37. КТ ребенка О., 2 года.
Поднадкостнично-эпидуральная гематома слева. Эпидуральная гематома затылочно-теменная область, поднадкостничная гематома – теменно-височная область. Умеренно выражен дислокационный синдром. При костной реконструкции видна область линейного перелома затылочной кости слева
с переходом на теменную кость.
Рис.7.38. КТ (А) и трехмерная реконструкция (Б) ребенка З., 2 года.
Растущий перелом затылочной и височной костей справа с формированием арахноидальной
экстра-интракраниальной кисты.
Б
Источник
Статьи
Опубликовано в журнале: “Практика педиатра” июнь, 2017г
И. Б. Миронов1, Е. В. Миронова2
Федеральное государственное бюджетное учреждение «Национальный научно-практический центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Министерства здравоохранения Российской Федерации, Москва.
1Врач-нейрохирург, член европейской ассоциации нейрохирургов (EANS).
2Врач-невролог, кандидат медицинских наук.
Статья посвящена актуальной проблеме современной неврологии – черепно-мозговой травме в детском возрасте. Представлены классификация форм, оценочные шкалы, клиническая картина и инструментальная диагностика черепно-мозговой травмы. Показано многообразие отдаленных последствий ЧМТ и возможные пути их медикаментозной коррекции у детей.
Ключевые слова: отдаленные последствия ЧМТ, астенический синдром, посттравматическая цефалгия, посткоммоционный синдром.
ВВЕДЕНИЕ
Актуальность проблемы исследования детской черепно-мозговой травмы обусловлена значительной распространенностью, высоким процентом инвалидизации и смертности детей. По данным ВОЗ отмечается постоянный рост частоты ЧМТ на 1-2% в год. Ряд авторов публикуют данные, что ЧМТ в детском возрасте встречается чаще, чем у взрослых пациентов. Это обусловлено рядом факторов: относительно большим размером головы у детей относительно тела, несовершенностью координации движений, большей активностью и любопытством детей. Данные о летальности при ЧМТ значительно варьируют в разных регионах Российской Федерации и составляют от 12-30% и более [1]. По данным НИИ Неотложной детской хирургии и травматологии, тяжелая ЧМТ составляет около 6% (среди детей, госпитализированных с нейротравмой), что соответствует 4000 инвалидов в год.
Следует отметить, что лечение последствий ЧМТ напрямую зависит от коррекции осложнений, требует применения высокотехнологичных методов лечения, дорогостоящих лекарственных препаратов и сопряжено со значительными экономическими потерями. Однако, несмотря на проведенное лечение, процент инвалидизации остается чрезмерно высоким. На данный момент в РФ отсутствует единый реестр детской и взрослой ЧМТ и ее поздних последствий. Это значительно усложняет статистический анализ общей распространенности и исходов заболевания. Сегодня в мире отсутствуют крупные мультицентровые исследования отдаленных последствий ЧМТ, касающиеся нейропротекции, нейрореанимации, нейрохирургии в детской практике. Следует отметить и положительные новости, касающиеся разработки группой авторов национальных рекомендаций по лечению пострадавших детей с ЧМТ [2], это первый в Российской Федерации документ, который строго регламентирует алгоритм действий при оказании медицинской помощи детям на разных этапах медицинской эвакуации вплоть до действий в специализированном стационаре с нейрохирургической службой.
Существует множество классификаций ЧМТ. Мы приведем наиболее часто используемые в повседневной практике врача. По степени тяжести ЧМТ классифицируется на легкую, средней тяжести и тяжелую. К ЧМТ легкой степени относится сотрясение головного мозга – функциональное нарушение нервной деятельности, которое характеризуется эпизодом травмы головы с дальнейшим развитием общемозговой (головная боль, тошнота, рвота) симптоматики. При инструментальной диагностике (краниографии в двух проекциях, КТ/МРТ головного мозга, нейросонографии) патологических изменений не выявляется. В литературе встречаются данные о повышении глиального нейроспецифического белка S-100 при ЧМТ [3], однако в повседневную практику данный биохимический анализ пока не вошел.
К ЧМТ средней тяжести относится ушиб головного мозга легкой степени. В клинической картине часто отмечается потеря сознания после удара по голове, доминирует общемозговая симптоматика и очаговые симптомы. При краниографии выявляются линии переломов, в грудном возрасте наиболее часто локализующиеся в теменных костях, существует особый вид вдавленных переломов по типу «целлюлоидного мячика», который требует экстренной нейрохирургической операции. При этом на КТ и МРТ подтверждаются костно-травматические изменения черепа, однако в веществе головного мозга изменений может и не быть. Ушиб головного мозга легкой степени всегда верифицируется при выявлении переломов костей свода и основания черепа.
ЧМТ тяжелой степени включает ушиб головного мозга средней и тяжелой степени, сдавление головного мозга, диффузное аксональное повреждение (ДАП). Вариабельность клинических проявлений обусловлена локализацией повреждения и стадией дислокационного синдрома. В клинической картине доминирует угнетение уровня бодрствования, стандартом оценки которого является бальная шкала комы Глазго (CGS) и присоединение очаговой симптоматики в виде гемипареза, анизокории, генерализованные и парциальные эпилептические приступы.
Рис 1. На краниограмме во фронтальной проекции визуализируется линейное просветление – линия перелома правой теменной кости. При клиническом осмотре определяется подкожная гематома в правой теменной области.
Баллы | Симптомы |
4 3 2 1 | Открывание глаз Произвольное На обращенную речь На болевой стимул Отсутствует |
6 5 4 3 2 1 | Двигательная реакция Выполняет команды Целенаправленная деятельность на болевой раздражитель Нецеленаправленная деятельность на болевой раздражитель Тоническое сгибание на болевой раздражитель Тоническое разгибание на болевой раздражитель Отсутствует |
5 4 3 2 1 | Речь Ориентированная и полная Спутанная Непонятные слова Нечленораздельные звуки Отсутствует |
При КТ/МРТ головного мозга выявляются значительные костные повреждения, ушибы вещества головного мозга с геморрагическим пропитыванием, внутричерепные гематомы, что требует экстренной нейрохирургической операции.
По распространению воздействия повреждающего фактора ЧМТ классифицируется как закрытая – без повреждения кожных покровов, открытая (проникающая/непроникающая). Открытая непроникающая ЧМТ характеризуется наличием повреждения кожных покровов и апоневроза с сохранением целостности твердой мозговой оболочки. При возникновении повреждения твердой мозговой оболочки и ликвореи, ЧМТ классифицируется как открытая проникающая. Данная классификация обусловлена высокой вероятностью возникновения инфекционных осложнений при открытой проникающей ЧМТ и требует превентивного назначения антибактериальных препаратов, проникающих через гематоэнцефалический барьер, для предотвращения бактериальных менингитов и энцефалитов – ургентных осложнений ЧМТ.
Рис 2. На КТ в аксиальной проекции визуализируются множественные очаги ушиба 3-4 типа (по В. Н. Корниенко) [4] лобных долей с геморрагической трансформацией, отмечается выраженный отек вещества головного мозга, компрессия желудочковой системы.
Общепринятым мировым стандартом оценки качества жизни пациентов, перенесших ЧМТ, является шкала исходов Глазго (Glasgow Outcome Scale, GOS) [6, 7]. Данной шкалой производится бальная оценка состояния пациента. Так, одному баллу соответствует смерть пациента, двум баллам – вегетативный статус, трем и четырем баллам соответствует тяжелая и умеренная инвалидизация, пяти баллам соответствует полное восстановление или с минимальным дефицитом. В практической работе врача часто используется расширенная шкала исходов Глазго, которая имеет более развернутый и уточненный характер оценки качества жизни пациентов.
Баллы | Исход |
1 | Смерть |
2 | Вегетативное состояние |
3 | Нейромышечная несостоятельность: пациент в сознании, однако тяжелая неврологическая симптоматика вынуждает продолжать лечение в отделении реанимации |
4 | Тяжелая несостоятельность: имеется грубый неврологический дефект, из-за которого пациенту необходим посторонний уход |
5 | Умеренная несамостоятельность: психический статус в пределах нормы. При этом пациент не в состоянии выполнять ряд необходимых действий. Нуждается в амбулаторном наблюдении |
6 | Легкая несамостоятельность: психический статус в пределах нормы. Больной сам себя обслуживает, может ходить сам или с посторонней поддержкой. Нуждается в специальном трудоустройстве |
7 | Хорошее восстановление: пациент постепенно возвращается к прежней жизни. Имеются незначительные неврологические нарушения. Передвигается самостоятельно |
8 | Полное восстановление |
В течение ЧМТ выделяют следующие периоды: острый период от 2 до 10 недель в зависимости от клинической формы ЧМТ; промежуточный период от 2 до 6 месяцев; отдаленный период (независимо от клинической формы): при клиническом выздоровлении – до 2 лет. Каждый из этих периодов характеризуется особенностями течения клинической картины [8]. Классификация последствий ЧМТ находится в стадии разработки [9]. На настоящий момент предложен усовершенствованный и расширенный вариант классификации с учетом патогенетических особенностей возникновения, преобладающих морфологических изменений, основного клинического синдрома и особенностей течения [10]. Из прямых последствий ЧМТ чаще встречаются церебрально-очаговый и астенический синдромы, гидроцефалия с гипертензионным синдромом.
Рис.3. Визуализируется эпидуральная гематома левой лобно-височно-теменной области с выраженным масс-эффектом и дислокацией вещества головного мозга.
Среди больных с давностью травмы от 4 месяцев до 5 лет по сравнению с получившими ее пять лет назад в три раза чаще наблюдались вестибулярные нарушения (у 18,1 и 6%). Уменьшается и число больных с афазией (с 9 до 5,9%). Непрямые последствия обычно формируются в результате легкой или среднетяжелой ЧМТ через месяцы или годы после травмы [11]. При этом важно отметить, что даже после легкой ЧМТ в отдаленном периоде могут сохраняться различные нарушения со стороны нервной системы. Примерно у 30% перенесших сотрясение головного мозга детей выявляется посткоммоционный синдром, который характеризуется головной болью, головокружением, нарушением сна, раздражительностью, повышенной утомляемостью, тревожностью, эмоциональной лабильностью, изменением поведения, вегетативной дисфункцией. При проведении специальных нейропсихологических методик выявляют снижение зрительной и слухоречевой памяти, внимания. Выраженность психоневрологических нарушений в отдаленном периоде ЧМТ во многом определяется степенью ее тяжести в остром периоде. Последствия ЧМТ оказывают значительное негативное влияние на психическое развитие детей, обусловливая нарушения интегративной деятельности головного мозга и препятствуя полноценной школьной и социальной адаптации.
Цереброваскулярные нарушения, психические дисфункции, вегетативные дисфункции, сочетание различных последствий требуют проведения коррекции с помощью медикаментозной терапии. С этой целью в моно- или комплексной терапии широко применяются лекарственные средства, сочетающие в себе ноотропный эффект с выраженным антиастеническим и церебропротективным действием.
Одним из эффективных лекарственных препаратов, используемых в комплексной терапии последствий ЧМТ, является деанола ацеглумат (Нооклерин, «ПИК-ФАРМА», Россия») – современный ноотропный препарат комплексного действия, обладающий структурным сходством с гамма-аминомасляной и глутаминовой кислотами, рекомендованный к применению у детей с 10 лет [12-15]. Нооклерин, являясь непрямым активатором метаботропных глутаматных рецепторов (3-го типа), предшественником холина и ацетилхолина, влияет на обмен нейромедиаторов в ЦНС, обладает нейропротекторной активностью, повышает энергообеспечение мозга и устойчивость к гипоксии, улучшает усвоение глюкозы нейронами, модулирует дезинтоксицирующую функцию печени [12-14]. В экспериментальных исследованиях показана высокая эффективность применения Нооклерина в качестве корректора гипоксических состояний, нарушений церебральной гемодинамики и метаболизма при ишемических и реперфузионных повреждениях мозга [19]. Препарат прошел широкое и многоплановое изучение в крупных медицинских центрах России (на 800 больных 8-ми клиник), и полученные при этом результаты свидетельствовали о значительном положительном влиянии Нооклерина на астенические (вялость, слабость, истощаемость, рассеянность, забывчивость) и адинамические расстройства [15-18]. Показано, что наиболее выраженную терапевтическую эффективность Нооклерин оказывает при астении (в 100% случаев), повышая активность поведения в целом и улучшая общий тонус и настроение [15], нивелируя таким образом последствия ЧМТ.
В подавляющем количестве публикаций подчеркивается хорошая переносимость Нооклерина и отсутствие нежелательных явлений на фоне его приема. Наряду с высокой терапевтической эффективностью эти свойства препарата определяют высокую приверженность терапии, в том числе у детей и подростков [20].
Список литературы:
1. Организационно-экономические и управленческие аспекты оказания медицинской помощи детям с черепно-мозговой травмой // Российский педиатрический журнал, 2010; 2
2. Лечение пострадавших детей с черепно-мозговой травмой //Клинические рекомендации, г. Казань, 2015: 3.
3. Талыпов А. Э., Пурас Ю. В., Годков М. А. и др. Исследование уровня протеина S-100 бета у пострадавших с черепно-мозговой травмой легкой тяжести // Нейрохирургия, 2011; 1
4. Корниенко В. Н., Васин Н. Я., Кузьменко В. А. Компьютерная томография в диагностике черепно-мозговой травмы. // М.: Медицина, 1987.
5. Крылов В.В., Пирадов М.А., Белкин А.А. и др. Шкалы оценки тяжести нарушений функций центральной нервной системы // Интенсивная терапия: Национальное руководство в 2-х т. под ред. Б. Р. Гельфанда, А. И. Салтанова // М.: ГЭОТАР-Медиа, 2011; Т. 1: 325.
6. Wilson J. T., Pettigrew L. E., Teasdale G. M. Structured interviews for the Glasgow Outcome Scale and the extended Glasgow Outcome Scale: guidelines for their use // J Neurotrauma, 1998; Vol. 15: 573-585
7. Wright J. Glasgow Outcome Scale – Extended // Encyclopedia of Clinical Neuropsychology / Kreutzer J. S., DeLuca J., Caplan B. eds.. – New York, Dordrecht, Heidelberg, London: Springer Science+Business , 2011: ISBN 978-0-387-79947-6.
8. Петрухин А.С. Неврология детского возраста // Медицина, М., 2004 : 638, 644.
9. Артарян А.А., Банин А.В, Гаевый О.В.
Клиническая классификация черепно-мозговой травмы у детей // Методические рекомендации. М., 1991: 17.
10. Немкова С. А., Заваденко Н. Н., Щедеркина И. О., Попов В. Е., Колтунов И. Е. Современные методы в комплексной реабилитации детей с последствиями инсульта, детским церебральным параличом и черепно-мозговой травмой //Фарматека, 2015; 11: 55
11. Макаров А. Ю. Последствия черепно-мозговой травмы и их классификация //Неврологический журнал, 2001;6(2): 38-42.
12. Морозов П. В. Новый отечественный ноотропный препарат «Нооклерин» (обзор) // Психиатрия и психофармакология, 2003; 5 (6): 262-267.
13. Медведев В. Э. Новые возможности лечения астенических расстройств в психиатрической, неврологической и соматической практике // Психиатрия и психофармакотерапия, 2013; 5 (4): 100-105.
14. Дикая В. И., Владимирова Т. В., Никифорова М. Д., Пантелеева Г. П. Отчет НЦПЗ РАМН. М.,1992.
15. Попов Ю. В. Применение Нооклерина у подростков в качестве антиастенического средства // Психиатрия и психофармакотерапия, 2004; 6 (4).
16. Александровский Ю. А., Аведисова А. С., Ястребов Д. В. и др. Применение препарата Ноо-клерин в качестве антиастенического средства у больных с функциональной астенией // Психиатрия и психофармакотерапия, 2003; 4: 164-166.
17. Мазур А. Г., Шпрехер Б. Л. Отчет по применению нового лекарственного препарата Деманол. М., 2008.
18. Сухотина Н. К., Крыжановская И. Л., Куприянова Т. А., Коновалова В. В. Нооклерин в терапии детей с пограничной психической патологией // Практика педиатра, 2011: 40-44.
19. Саврасова Т. В. Влияние ЛБК-149 и но-оклерина на некоторые метаболические показатели при ишемическом повреждении головного мозга в условиях дислипидемии. Дисс. канд. мед. наук, 2005.
20. Медведев В. Э. Новые возможности лечения астенических расстройств в психиатрической, неврологической и соматической практике // Психиатрия и психофармакотерапия, 15; 4: 105.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
