Ушиб мозга с субарахноидальным кровоизлиянием последствия
Любая геморрагия в мозг может привести к летальному исходу. Субарахноидальное кровоизлияние – одно из самых опасных для человека: приблизительно половина пациентов погибает еще до приезда в больницу или во время операции. Однако даже если человека вылечили, болезнь не проходит бесследно. Итак, какие проблемы со здоровьем может получить пациент, переживший подобное кровотечение?
Что такое субарахноидальное кровотечение (САК), его симптоматика и диагностика
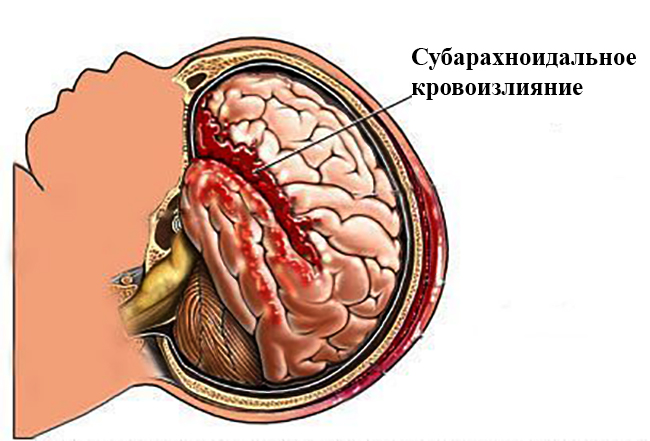
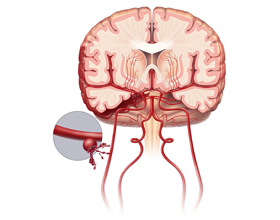
САК – это кровоизлияние в пространство между паутинной и мягкой мозговыми оболочками. Наиболее частыми его причинами являются разрыв аневризмы или получение травмы. Симптомы кровоизлияния появляются без предпосылок: голова внезапно начинает болеть, словно от удара тупым предметом, появляется ощущение тошноты, человек неоднократно теряет сознание. Диагностируют заболевание с помощью компьютерной томографии, реже – люмбальной пункцией.

Последствия субарахноидального кровотечения
- Нейрокогнитивные расстройства. Большая часть пациентов, переживших САК, страдают психическими расстройствами, даже если до болезни таких проблем не наблюдалось. К наиболее распространенным последствиям относятся депрессия, посттравматические расстройства и нарушения когнитивных функций. По этой причине людям, перенесшим кровоизлияние, нужно посетить психолога в период реабилитации, даже если лечебное заведение не направило пациента на подобную консультацию. Помимо этого, большинству людей назначают антидепрессанты после проведения операции, поэтому поинтересуйтесь у своего лечащего врача, назначены ли подобные лекарства.
- Повреждение гипоталамуса и гипофиза. Если САК произошло из-за разрыва аневризмы, велика вероятность повреждения гипоталамуса и гипофиза, центров гормональной регуляции человека. У 25 процентов людей наблюдаются проблемы с выработкой определенных гормонов, чаще всего соматропина, фолликулостимулирующего и лютеинизирующего. Проблемы с первым окажут влияние преимущественно на детей и подростков: их рост замедлится или остановится; повреждение второго и третьего пагубно воздействует на репродуктивную систему человека. Пациентов после проведения операции обычно направляют на консультацию к эндокринологу.
- Инвалидизация. Из-за повреждения некоторые зоны мозга могут быть травмированы, что приводит к ухудшению выполнения некоторых функций. К этому относится как пребывание человека в вегетативном состоянии, так и ухудшение функциональности некоторых мышц и конечностей. Большинство пациентов проходят эту стадию в разной степени тяжести после операции, потому что головному мозгу требуется время на восстановление после болезни. Во время реабилитации многим людям удается улучшить свое состояние и избежать таких тяжелых последствий, как паралич конечностей или пребывание в вегетативном состоянии.
- Эпилепсия. Если САК было получено в результате черепно-мозговой травмы, существует риск развития эпилепсии. Эта болезнь характеризуется припадками, которые включают в себя судороги, в некоторых случаях еще обмороки, прикусывание языка и ретроградную амнезию (человек не помнит ничего о приступе). Чаще всего это последствие выявляется еще в стационаре, однако известны случаи, когда симптом проявлялся у пациентов спустя месяц и более после травмы. Припадки неконтролируемы, и единственное, что может сделать врач во время приступа – ждать, пока судороги закончатся и уже потом вводить необходимые лекарства.
- Гидроцефалия. Гидроцефалия –заболевание, характеризующееся накоплением цереброспинальной жидкости в желудочках головного мозга. Признаками этого осложнения являются головные боли (чаще всего по утрам), тошнота, иногда рвота. В отличии от новорожденных пациентов размер головы взрослого человека не увеличивается. Обнаружить эту патологию можно с помощью компьютерной, реже – магнитно-резонансной томографии. При выявлении заболевания человека готовят к экстренной операции и при своевременном вмешательстве пациент пойдет на поправку и выздоровеет.
- Ишемия. Ишемия – осложнение, характеризующееся снижением кровоснабжения. Это происходит по причине сужения сосудов. У пациента нарушается обмен веществ, это сопровождается гипоксией и на последней стадии начинается ишемический некроз ткани. Эта патология может привести к летальному исходу, если вовремя не начать лечение. Однако процесс является обратимым, и при должном медицинском уходе пациент может восстановиться.
- Менингит. Перенесенное кровоизлияние повышает риск появления менингита у пациента. Это заболевание характеризуется воспалением мягких мозговых оболочек. Первыми симптомами являются повышение температуры, рвота, судороги, мучительные головные боли. Если кровоизлияние произошло из-за травмы, существует риск занести инфекцию во время ранения, что приведет к началу воспаления. На ранних стадиях это опасное заболевание можно вылечить с помощью антибиотиков.
- Отек мозга. Отек происходит по причине накопления жидкости в клетках мозга. Объем органа увеличивается, что сопровождается головными болями, тошнотой и обмороками. Для лечения болезни врачам необходимо поддерживать нормальную температуру и оксигенацию пациента, назначить диуретики, а также ликвидировать причины, нарушающие венозный отток крови от черепа. Эту патологию нужно устранить как можно быстрее, потому что игнорирование симптомов может привести к летальному симптому.
Вывод
При наличии подобных последствий обязательно проконсультируйтесь с врачом об их устранении. Не ожидайте, что симптомы сами пройдут и не занимайтесь самолечением. Игнорирование подобных проблем приводит многих пациентов к тому, что легко устранимые последствия на раннем этапе переходят в болезни на запущенных стадиях, которые сложно, а иногда и невозможно вылечить.
Источник
К субарахноидальным кровоизлияниям относят возникшее в результате травмы скопление крови и/или ее свертков в субарахноидальном пространстве, обусловливающее нарушения циркуляции и резорбции ликвора, вазоспазм, раздражение мягких мозговых оболочек и коры головного мозга.
ЭПИДЕМИОЛОГИЯ
Травматические субарахноидальные кровоизлияния (ТСАК) наиболее частый вид внутричерепных кровоизлияний. Ранее об этом свидетельствовали данные больших серий аутопсий. В настоящее время распространенность (ТСАК) подтверждают методы нейровизуализации головного мозга. Н.М. Eisenberg et al. на основе анализа первичных КТ данных у 753 больных с тяжелой ЧМТ выявили наличие ТСАК у 39% пострадавших. A. Kakarieka. et al. по материалам европейского мультицентрового исследования (819 пациентов) обнаружили КТ признаки ТСАК более чем у 32% пострадавших с тяжелой ЧМТ. ТСАК оказалась самой частой патологией на КТ по данным J.S. Jeret et al. в серии 712 наблюдений больных со среднетяжелой ЧМТ. N. Fukuda et al., в группе 123 больных с тяжелой диффузной травмой мозга диагностировали ТСАК в первые 24 часа по КТ у 99 пациентов. Частота наблюдений ТСАК по данным КТ варьирует в широких пределах от 8% до 59%.
Возрастные факторы при ТСАК не являются определяющими, однако отмечается тенденция нарастания частоты кровоизлияний с возрастом пострадавших.
Алкогольная интоксикация способствует увеличению риска ТСАК.
МЕХАНИЗМЫ ОБРАЗОВАНИЯ
ТСАК рассматривают, как результат непосредственного повреждения сосудов, располагающихся в субарахноидальном пространстве (артериальных или венозных веточек, мельчайших пиальных артерий), покрывающем на всем протяжении поверхность мозга. Излившаяся в субарахноидальное пространство кровь распространяется по ликвороносным каналам, субарахноидалъным ячеям, цистернам. При этом происходит удаление значительного количества излившейся крови с оттекающим из субарахноидального пространства ликвором.
В ряде случаев ТСАК обусловлены артериальным кровотечением в зонах массивных ушибов мозга.
Другим пусковым механизмом ТСАК может являться комплекс тяжелых вазомоторных нарушений, сопровождающих течение ЧМТ.
ПАТОГЕНЕЗ И ПАТОМОРФОЛОГИЯ
Кровоизлияние, развивающееся в субарахноидальном пространстве, воздействует, в первую очередь, на паутинную и мягкую (сосудистую) оболочки, структуры субарахноидального пространства, адветицию артерий. Особенности локализации и течения ТСАК прежде всего сопряжены с развертыванием патологии системы ликворообращения. Патоморфологические изменения, связанные с наличием крови в субарахноидальном пространстве, зависят не только от сроков с момента травмы, но и от массивности ТСАК. Выделяют морфологические типы ТСАК с нарушением и сохранностью мягкой мозговой оболочки. Нарушения лептоменингса при ТСАК могут носить разрывной и эрозивный вид. Разрывные повреждения мягких мозговых оболочек встречаются только в месте переломов костей черепа, сопровождающихся разрывами твердой мозговой оболочки. Эрозивные повреждения чаще наблюдаются при травме ускорения и при сдавлении головы. При целостности оболочки наблюдаются пятнистые и ограниченно диффузные ТСАК. Они обычно располагаются на месте приложения удара или на противоположной стороне, как правило, небольших размеров. Диффузные ТСАК могут распространяться по всей поверхности обоих полушарий, поверхности мозжечка и заполнять кровью цистерны основания мозга.
Реактивные изменения мозговых оболочек в ответ на излившуюся кровь развиваются уже через 1—4 часа — отмечается концентрация полиморфных лейкоцитов вокруг кровеносных сосудов с последующей в течение 4—16 ч инфильтрации ими мягкой мозговой оболочки. В дальнейшие 16—32 ч увеличивается число лейкоцитов и лимфоцитов, наблюдаются явления фагоцитоза. Полиморфноклеточная реакция достигает наибольшего развития на третьи сутки с преобладанием лейкоцитов и нарастающего фагоцитоза. Прохождение эритроцитов через паутинную оболочку сопровождаются расширением межклеточных пространств с деструкцией демосом и реакцией арахноидальных клеток. Разнообразная форма и пластичность эритроцитов способствует их проникновению через клеточные пласты паутинной оболочки, способствуя ее разрыхлению и деформации.
Ультраструктурные изменения мягкой мозговой оболочки выявляют нарушения наружного эндотелиального слоя обращенного в субарахноидальное пространство, разрыхление коллагеноволокнистой основы оболочки, разрыхление микрофибрилл осмиофильного компонента базальной мембраны на границе с мозгом. Нарушения морфологического субстрата мягкой мозговой оболочки приводят к нарушениям ликворотканевого барьера. Таким образом, выведение компонентов крови из субарахноидального пространства сопровождается нарушениями ультраструктуры морфологических субстратов барьеров между ликвором и пограничными с ними средами и тканями.
К 8—10 сут обнаруживаются признаки организации ТСАК с явлениями фиброза мягких мозговых оболочек. Фиксация элементов крови в защитнотрофической системе субарахноидального пространства способствует загрузке мягкой мозговой оболочки продуктами их распада. Накопление их является своеобразным раздражителем, вызывающим развитие хронического асептического лептоменингита, спаечного процесса в субарахноидальном пространстве с последующими нарушениями циркуляции ликвора, что, в свою очередь, ведет к развитию гидроцефалии.
Течение ТСАК отражает три последовательно протекающие стадии:
1) излившаяся в субарахноидальное пространство кровь распространяется от места кровоизлияния по системам ликвороносных каналов, достигая выделительных каналов на вершинах извилин, одновременно проникая через отверстия в стенках каналов в субарахноидальные ячеи. Появление кро ви в субарахноидальном пространстве приводит к увеличению объема ликвора с последующей ост рой ликворной гипертензией. Повышение ликворного давления способствует усилению оттока ликвора из субарахноидального пространства. С момента травмы, в первые часы, сутки наблюдается интенсивное удаление с ликвором эритроцитов и других компонентов крови за пределы субарахнои дального пространства, что способствует частичной санации ликвора;
2) свертывание крови в ликворе с образовани ем свертков. Установлено, что кровь в ликворесвертывается в разведении 1:100 и более. В этих услови ях в субарахноидальном пространстве формируются свертки крови, приводящие к частичной или пол ной блокаде отдельных или нескольких цистерн и ликвороносных каналов. Эти нарушения влекут за собой дальнейшие нарушения ликвороциркуляции, с нарастающей ликворной гипертензией. Одновременно с этим имеют место нарушения оттока ликвора за пределы субарахноидального пространства в выделительных каналах лептоменингса. Это, в свою очередь, ведет к нарушению процесса удале ния компонентов крови из субарахноидального пространства. Формирующиеся свертки располагаются преимущественно в системах цистерн и ликвороносных каналов, в местах переплетения паравазальных структур. В процессе свертывания крови часть тромбоцитов распадается с высвобождением серотонина, обладающего выраженным сосудосуживающим действием. В системе субарахноидальных ячей также происходит задержка форменных элементов крови и их фиксация. Начиная с 2—3 сут начинается фагоцитоз компонентов свертков крови арахноидальными клетками и макро фагами, что способствует санации ликвора и нормализации его состава;
3) лизис свертков крови вследствие фибринолитической активности арахноидальных клеток, повсеместно выстилающих субарахноидальное пространство. Лизис свертков приводит к постепенному полному или частичному восстановлению ликвороциркуляции и резорбции ликвора. Степень этих нарушений находится в определенной зависимости от массивности ТСАК.
Таким образом представления о санации ликвора при ТСАК предполагают следующие механизмы очищения ликвора: 1. Выведение излившейся крови с оттекающим ликвором за пределы субарахноидального пространства; 2. Фиксация элементов крови в защитно-трофической системе мягкой мозговой оболочки.
Излившаяся в субарахноидальное пространство кровь, по данным ангиографии в 5%—41% случаев сопровождается развитием сосудистого спазма. Транскраниальная доплерография, определяющая вазоспазм, при скорости линейного мозгового кровотока, превышающего >120 см/сек, наблюдается у 27—50% пострадавших с ЧМТ. В основе вазоспазма лежит целый комплекс причин: механические факторы, воздействие продуктов гемолиза и фибринолиза форменных элементов крови и ее свертков, наушения баланса кальция, простогландинов, их дериватов и других биохимических нарушений. Вазоспазм — одна из основных причин развития вторичных ишемических неврологических нарушений у больных с ТСАК и прогностически является неблагоприятным фактором течения острого периода ЧМТ.
КЛИНИКА
В клинической картине ТСАК характерно сочетание общемозговой, менингеальной и очаговой неврологической симптоматики. У пострадавших с ТСАК отмечаются интенсивные головные боли. Они часто носят оболочечный характер, преимущественно локализуясь в области лба, надбровных дуг и затылка. По данным Г.Е. Педаченко, у 47% пострадавших с ТСАК выявляется синдром мозжечкого намета. Головные боли усиливаются при движение головой, напряжении и перкуссии черепа. Нередко с головной болью сочетаются головокружение, тошнота, рвота, вегетативные нарушения. Последние проявляются потливостью, похолоданием конечностей, побледненисм кожных покровов, снижением ранее повышенной температуры, колебаниями артериального давления.
Общемозговая симптоматика нередко сопровождается психопатологическими симптомами в виде психомоторного возбуждения, дезориентировки и
спутанности. Угнетение сознания проявляется в виде умеренного и/или глубокого оглушения, сопора длительностью до 3—7 суток. Восстановление сознания обычно протекает на фоне длительно наблюдаемых после ЧМТ астеновегетативного синдрома и нарушений памяти, чаще в виде ретро и антероградной амнезии, корсаковского синдрома и др. Выраженность изменений памяти зависит от тяжести ЧМТ.
К характерным клиническим проявлениям ТСАК относится менингеальная симптоматика. Ее развитие связывают с раздражением мозговых оболочек излившейся кровью и продуктами ее распада. Мснингсальные симптомы (светобоязнь, болезненное ограничение движений глазных яблок, ригидность затылочных мышц, симптомы Кернига, Брудзинского и др.) выявляются у большинства больных. Выраженность клинических признаков оболочечного раздражения часто отражает массивность ТСАК. Менингеальные симптомы обычно нарастают на протяжении первых нескольких суток после ЧМТ Регресс менигеальной симптоматики наступает в более поздние сроки по сравнению с санацией ликвора, на 14—21 сут при благоприятном течении ЧМТ.
Симптомы очагового поражения головного мозга при ТСАК разнообразны и могут быть обусловлены раздражением корковых отделов мозга, скоплением крови вне очагов ушиба, так и повреждениями мозга. Так, при локализованных ТСАК очаговая симптоматика может проявляться легкой недостаточностью VII и XII черепно-мозговых нервов по центральному типу, анизорефлексией, мягкой пирамидной недостаточностью. При массивных ТСАК очаговая неврологическая симптоматика может носить четкий и стойкий характер, при этом ее выраженность зависит от обширности и локализации повреждения мозга.
Одной из особенностей течения ТСАК являются нарушения терморегуляции. Нередко наблюдаются значительные колебания температуры тела в пределах 1—2 недели.
ДИАГНОСТИКА
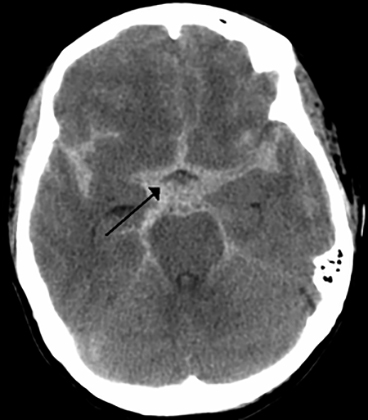
Прямая визуализация ТСК доступна при использовании КТ (рис. 14—1; см. также рис. 27—9). Признаком ТСАК является повышение плотности в области базальных цистерн, боковой щели и субарахноидальных пространств. Примесь крови в ликворс на КТ выявляется, если се концентрация является достаточно высокой для повышения коэффициента адсорбции ликвора. Наиболее четкая КТ верификация
Рис. 14—1. КТ. 1 сутки после ЧМТ средней степени тяжести: А — субарахноидальное кровоизлияние локализующееся в базальных цистернах (межножковая, охватывающая цистерны); Б — субарахноидальное кровоизлияние локализующееся в левой боковой и межполушарной щелях
ТСАК возможно только в раннем периоде. По данным A. Kakarieka, признаки ТСАК по первичным КТ (среднее время проведения 4 часа после ЧМТ) выявляются у 33% пострадавших. При этом ТСАК наиболее часто визуализируются в области конвекситальной поверхности головното мозга (у 70%), субарахноидальных шелей (у 53%) и реже в области базальных цистерн (у 33%). Возможна также КТ оценка массивности ТСАК, определяемая по балльной системе отражающей, распространенность крови по ликворосодсржащим пространствам. Массивность ТСАК снижается на 50% при проведении повторной КТ в пределах первых двух суток после ЧМТ и составляет на третьи сутки лишь одну треть от оценки ее в первые часы. Визуализация динамики ТСАК подчеркивает необходимость раннего проведения КТ после ЧМТ с целью его верификации. Ограничение возможностей КТ в определении ТСАК чаще всего бывает обусловлено низкой разрешающей способностью аппаратуры и временными параметрами исследования.
Эффективность МТР в диагностике острых ТСАК неоднозначна. Примесь крови в ликворе очень незначительно повышает сигнал на томограммах в режиме Т1 и минимально понижает в режиме Т2. МРТ гораздо точнее КТ выявляет ТСАК в подострой и хронической стадиях, когда кровь или даже ее следы за счет наличия метгемоглобина, играют роль естественного контраста и обеспечивают высокий сигнал на томограммах по Т1 и Т2 (поверхностный сидероз).
Рутинная диагностика ТСАК основана на результатах люмбалъной пункции, выявляющей наличие кровянистой окраски ликвора. Этот признак подтверждает факт ТСАК, разумеется за исключением ситуаций связанных с путевой кровью. Дополнительным признаком ТСАК также является ксантохромия ликвора, обусловленная гемолизом, и наблюдаемая в 10% случаев уже в первые сутки после ЧМТ. Наибольшей интенсивности она достигает на 3—5 сут и наблюдается в пределах 1—3 нед после ЧМТ. Плеоцитоз ликвора, как реакция на излившуюся кровь, обычно с преобладанием нейтрофилов, постоянно сопровождает течение ТСАК. Выраженность его проявлений разнообразна и связана с индивидуальной реактивностью оболочек головного мозга. Характерным ликворологическим тестом при ТСАК является изменение белкового состава ликвора, обусловленного не только поступлением с излившейся кровью, но и дисгемическими нарушениями.
Массивность ТСАК часто отражает тяжесть ЧМТ. Так, при ушибах мозга легкой степени количество эритроцитов в 1 мм3 ликвора может колебаться от нескольких сотен до 8—10 тысяч; при ушибах мозга средней степени от нескольких десятков тысяч до 100—200 тысячи выше; при тяжелых ушибах от нескольких сотен до 1 млн и более эритроцитов в 1 мм3.
Диагностическая оценка количества эритроцитов в ликворе требуют обязательного учета клинической картины ЧМТ.
ЛЕЧЕНИЕ
Лечебные мероприятия при ТСАК направлены на остановку кровотечения, нормализацию внутричерепного давления, удаление излившейся крови, продуктов ее распада и профилактику осложнений.
Консервативная терапия включает назначение гемостатических средств (дицинон, аминокалроновая кислота, глюконат кальция и др), дегидратационной терапии под контролем водноэлектролитного баланса (осмотические диуретики, салуретики), противовоспалительной терапии по показаниям (открытая проникающая ЧМТ — антибиотики широкого спектра действия, перекрывающие граммположительную и граммотрицательную микрофлору); сосудистая терапия и ноотропы. Профилактически проводится противосудорожная терапия. Использование в лечении ТСАК антагонистов кальция (нимодипин) по данным международных кооперативных исследований (HIT I—IV trials) не сопровождается достоверными результатами, однако отмечается улучшение исходов ТСАК в группе больных, длительно (21 день) получавших препарат. Комплексное лечение дополняется по мере необходимости симптоматическими препаратами (анальгетики, седативные препараты, витамины и др.). Пострадавшие должны строго соблюдать постельный режим.
Для санации ликворных пространств с удалением излившейся крови и продуктов ее распада используют периодические люмбальные пункции. При этом очищение ликвора наблюдается в сроки 7—14 сут. Наряду с рутинными методами очищения ликворных пространств, разработаны интенсивные методы санации. Они показаны при массивных ТСАК у пострадавших без признаков внутричерепных травматических объемных образований, отека мозга и дислокационных проявлений. В основу их положено постоянное дренирование ликворных пространств с контролируемым выведением ликвора или его частичным замещением (дренирование субарахноидального пространства с установкой люмбального дренажа; дренирование ликворных пространств на разных уровнях с промыванием ликворозамещающими растворами).
Ранее широко используемые методы эндолюмбального введения воздуха, кислорода, озона, лидазы и других препаратов в настоящее время оставлены в связи с отсутствием достоверных сведений о положительном влиянии этих методов на исходы ТСАК, и нередко возможностью тяжелых осложнений.
ПРОГНОЗ И ИСХОДЫ
ТСАК относится к неблагоприятным факторам при ЧМТ. На течение и исходы повреждений мозга влияют массивность ТСАК и их локализация, выявляемые на первичных КТ исследованиях. Возраст пострадавших, алкогольная интоксикация при ТСАК также отражаются на исходах ЧМТ.
На фоне легкой ЧМТ наблюдается хорошее восстановление у большинства пострадавших с ТСАК.
При травме средней степени тяжести ТСАК существенно отражаются на увеличение количества неблагоприятных исходов. В частности посттравматическая эпилепсия развивается у пострадавших после ТСАК в два раза чаще, чем без него.
Плохие исходы включающие летальные случаи, вегетативное состояние, грубую инвалидизацию в два раза чаще наблюдаются у пострадавших с тяжелой ЧМТ, сопровождаемой ТСАК, чем без него.
А.Д. Кравчук, Г.Ф. Добровольский
Опубликовал Константин Моканов
Источник
